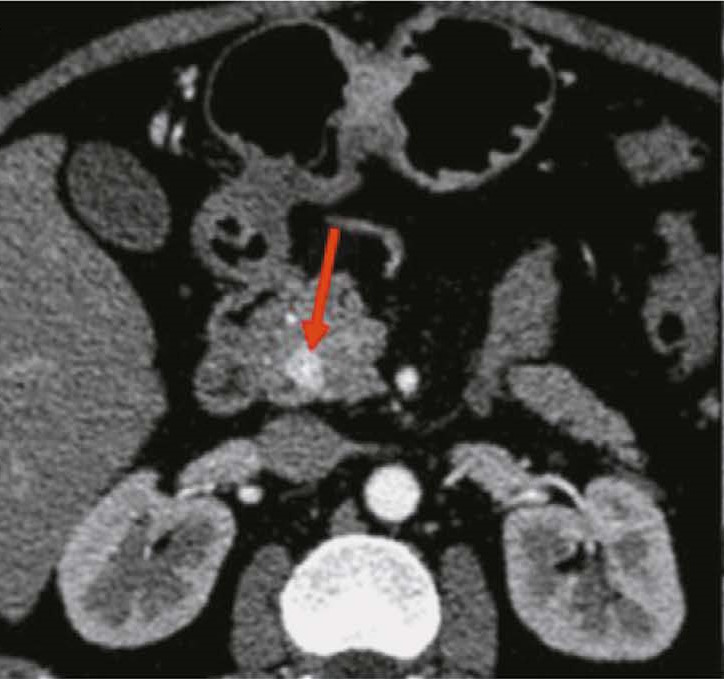
Neuroendocrine tumors of stomach and pancreas: diagnostic potential of radiomics, issues, and solutions
- Autores: Nudnov N.V.1,2,3, Shakhvalieva E.S.4, Karelidze D.G.4, Borisov A.A.4, Ivannikov M.E.4
-
Afiliações:
- Russian Research Center of Roentgenology and Radiology, Moscow, Russia
- Russian Medical Academy of Continuing Professional Education
- RUDN University
- Russian Research Center of Roentgenology and Radiology
- Edição: Volume 5, Nº 4 (2024)
- Páginas: 712-724
- Seção: Original Study Articles
- URL: https://bakhtiniada.ru/DD/article/view/309831
- DOI: https://doi.org/10.17816/DD629345
- ID: 309831
Citar
Resumo
BACKGROUND: Radiomics is currently a promising and prospective tool for diagnosing and treating neuroendocrine neoplasms at various sites. This method is often used for differential diagnosis of gastrointestinal neuroendocrine tumors with other neoplasms at this site.
AIM: The aim of the study was to evaluate the potential of radiomics for differential diagnosis of neuroendocrine tumors of stomach and pancreas.
MATERIALS AND METHODS: The study included data of 12 patients with morphologically proven neoplasms of the stomach (6 with neuroendocrine tumors and 6 with adenocarcinomas) and data of 22 patients with morphologically proven neoplasms of the pancreas (11 with neuroendocrine tumors and 11 with adenocarcinomas). All patients underwent abdominal computed tomography (CT) with intravenous contrast enhancement prior to treatment at the Russian Scientific Center of Roentgenology and Radiology. Radiomics parameters were calculated for the area of gastric and pancreatic tumor manually segmented in the native phase of the CT scan. The results were processed and statistically analyzed using Microsoft Office Excel and R-Studio, a free, open-source software development environment for the R programming language.
RESULTS: CT scan examples demonstrate typical and atypical visual signs of neuroendocrine tumors of stomach and pancreas, contrast enhancement characteristics, location and structure of neoplasms. Fifteen radiomics parameters were identified that were statistically significantly different between gastric neuroendocrine tumor and gastric adenocarcinoma. In pancreas, neuroendocrine tumors differed significantly from adenocarcinomas in 14 radiomics parameters.
CONCLUSIONS: Neuroendocrine tumors of stomach and pancreas are rare neoplasms that are mostly asymptomatic and difficult to visualize due to their small size and contrast enhancement characteristics. Texture analysis may be a promising approach to differentiate gastrointestinal neuroendocrine tumors from other neoplasms at these sites, especially in the view of the difficulty in obtaining a biopsy.
Texto integral
##article.viewOnOriginalSite##Sobre autores
Nikolay Nudnov
Russian Research Center of Roentgenology and Radiology, Moscow, Russia; Russian Medical Academy of Continuing Professional Education; RUDN University
Autor responsável pela correspondência
Email: nudnov@rncrr.ru
ORCID ID: 0000-0001-5994-0468
Código SPIN: 3018-2527
MD, Dr. Sci. (Medicine), Professor
Rússia, Moscow; Moscow; MoscowElina Shakhvalieva
Russian Research Center of Roentgenology and Radiology
Email: shelina9558@gmail.com
ORCID ID: 0009-0000-7535-8523
Rússia, Moscow
David Karelidze
Russian Research Center of Roentgenology and Radiology
Email: david_ka@mail.ru
ORCID ID: 0009-0002-0375-1291
Rússia, Moscow
Aleksandr Borisov
Russian Research Center of Roentgenology and Radiology
Email: aleksandrborisov10650@gmail.com
ORCID ID: 0000-0003-4036-5883
Código SPIN: 4294-4736
Rússia, Moscow
Mikhail Ivannikov
Russian Research Center of Roentgenology and Radiology
Email: ivannikovmichail@gmail.com
ORCID ID: 0009-0007-0407-0953
Código SPIN: 3419-2977
Rússia, Moscow
Bibliografia
- Shah MH, Goldner WS, Benson AB, et al. Neuroendocrine and Adrenal Tumors, Version 2.2021, NCCN Clinical Practice Guidelines in Oncology. J Natl Compr Canc Netw. 2021;19(7):839–868. doi: 10.6004/jnccn.2021.0032
- Menshikov KV, Sultanbaev AV, Musin ShI, et al. Neuroendocrine Tumours: a Literature Review. Creative surgery and oncology. 2021;11(2):174–182. EDN: RTJQRK doi: 10.24060/2076-3093-2021-11-2-174-182
- Alekberzade AV, Krylov NN, Lipnitskiy EM, et al. Gastric neuroendocrine tumors. Pirogov Russian Journal of Surgery. 2019;(12):111–120. EDN: RIRQGH doi: 10.17116/hirurgia2019121111
- Ministry of Health of the Russian Federation. Clinical guidelines «Neuroendocrine tumors» [Internet]. 2020. Available from: https://cr.minzdrav.gov.ru/schema/610_1 (In Russ.) Accessed 2024 Mar 4.
- Dasari A, Shen C, Halperin D, et al. Trends in the Incidence, Prevalence, and Survival Outcomes in Patients With Neuroendocrine Tumors in the United States. JAMA Oncol. 2017;3(10):1335–1342. doi: 10.1001/jamaoncol.2017.0589
- Department of Health of the City of Moscow. Guidelines «Neuroendocrine tumors of the pancreas» [Internet]. 2019. Available from: https://niioz.ru/upload/iblock/4ee/4ee9895614aa276f538069caee698fce.pdf (In Russ.) Accessed 2024 Mar 4.
- Halfdanarson TR, Rabe KG, Rubin J, Petersen GM. Pancreatic neuroendocrine tumors (PNETs): incidence, prognosis and recent trend toward improved survival. Ann Oncol. 2008;19(10):1727–1733. doi: 10.1093/annonc/mdn351
- Loosen SH, Kostev K, Jann H, et al. Distribution of gastrointestinal neuroendocrine tumors in Europe: results from a retrospective cross-sectional study. J Cancer Res Clin Oncol. 2023;149(4):1411–1416. doi: 10.1007/s00432-022-04003-3
- Chernousov AF, Egorov AV, Musaev GKh, et al. Neuroendocrine tumors of a pancreas: 30 year’s experience of clinic of faculty surgery of N.N. Burdenko. Pirogov Russian Journal of Surgery. 2013;(7):13–19. EDN: QYSJLV
- Dias AR, Azevedo BC, Alban LBV., et al. Gastric neuroendocrine tumor: review and update. Arq Bras Cir Dig. 2017;30(2):150–154. doi: 10.1590/0102-6720201700020016
- Sundin A, Vullierme MP, Kaltsas G, Plöckinger U. ENETS Consensus Guidelines for the Standards of Care in Neuroendocrine Tumors: radiological examinations. Neuroendocrinology. 2009;90(2):167–183. doi: 10.1159/000184855
- Radiographia.info [Internet]. Pancreatic endocrine tumors. Available from: https://radiographia.info/article/endokrinnyeopuholipodzheludochnoyzhelezy (In Russ.) Accessed: 04.03.2024
- Gruzdev IS. Application of texture analysis for differential diagnosis and prognosis in the surgical treatment of hypervascular pancreatic masses [dissertation]. Moscow; 2022. Available from: https://www.rncrr.ru/nauka/dissertatsionnyysovet/obyavleniyaozashchitakh/upload%202023/Груздев_диссертация.pdf (In Russ.) EDN: BKPRVN
- Lewis RB, Lattin Jr GE, Paal E. Pancreatic endocrine tumors: radiologic clinicopathologic correlation. Radiographics. 2010;30(6):1445–1464. doi: 10.1148/rg.306105523
- Raman SP, Hruban RH, Cameron JL, et al. Pancreatic imaging mimics: part 2, pancreatic neuroendocrine tumors and their mimics. AJR Am J Roentgenol. 2012;199(2):309–318. doi: 10.2214/AJR.12.8627
- Sahani DV, Bonaffini PA, Fernández Del Castillo C, Blake MA. Gastroenteropancreatic neuroendocrine tumors: role of imaging in diagnosis and management. Radiology. 2013;266(1):38–61. doi: 10.1148/radiol.12112512
- Ganeshan D, Bhosale P, Yang T, Kundra V. Imaging features of carcinoid tumors of the gastrointestinal tract. AJR Am J Roentgenol. 2013;201(4):773–786. doi: 10.2214/AJR.12.9758
- Mikhailov IV, Beliakouski VN, Kudrashou VA, et al. Biopsy of pancreatic tumors prior to resection: for and against. Health and Ecology Issues. 2021;18(1):62–69. EDN: ECTEZT doi: 10.51523/2708-6011.2021-18-1-9
- Staal FCR, Aalbersberg EA, van der Velden D, et al. GEP-NET radiomics: a systematic review and radiomics quality score assessment. Eur Radiol. 2022;32(10):7278–7294. doi: 10.1007/s00330-022-08996-w
- van Griethuysen JJM, Fedorov A, Parmar C, et al. Computational Radiomics System to Decode the Radiographic Phenotype. Cancer Res. 2017;77(21):e104–e107. doi: 10.1158/0008-5472.CAN-17-0339
- Wang X, Qiu JJ, Tan CL, et al. Development and Validation of a Novel Radiomics-Based Nomogram With Machine Learning to Preoperatively Predict Histologic Grade in Pancreatic Neuroendocrine Tumors. Front Oncol. 2022;12:843376. doi: 10.3389/fonc.2022.843376
- Dong Y, Yang DH, Tian XF, et al. Pancreatic neuroendocrine tumor: prediction of tumor grades by radiomics models based on ultrasound images. Br J Radiol. 2023;96(1149):20220783. doi: 10.1259/bjr.20220783
- Ye JY, Fang P, Peng ZP, et al. A radiomics based interpretable model to predict the pathological grade of pancreatic neuroendocrine tumors. Eur Radiol. 2024;34(3):1994–2005. doi: 10.1007/s00330-023-10186-1
- Chiti G, Grazzini G, Cozzi D, et al. Imaging of Pancreatic Neuroendocrine Neoplasms. Int J Environ Res Public Health. 2021;18(17):8895. doi: 10.3390/ijerph18178895
- Liang W, Yang P, Huang R, et al. A Combined Nomogram Model to Preoperatively Predict Histologic Grade in Pancreatic Neuroendocrine Tumors. Clin Cancer Res. 2019;25(2):584–594. doi: 10.1158/1078-0432.CCR-18-1305
- Wang R, Liu H, Liang P, et al. Radiomics analysis of CT imaging for differentiating gastric neuroendocrine carcinomas from gastric adenocarcinomas. Eur J Radiol. 2021;138:109662. doi: 10.1016/j.ejrad.2021.109662
- Han X, Yang J, Luo J, et al. Application of CT-Based Radiomics in Discriminating Pancreatic Cystadenomas From Pancreatic Neuroendocrine Tumors Using Machine Learning Methods. Front Oncol. 2021;11:606677. doi: 10.3389/fonc.2021.606677
- Shi YJ, Zhu HT, Liu YL, et al. Radiomics Analysis Based on Diffusion Kurtosis Imaging and T2 Weighted Imaging for Differentiation of Pancreatic Neuroendocrine Tumors From Solid Pseudopapillary Tumors. Front Oncol. 2020;10:1624. doi: 10.3389/fonc.2020.01624
- Li X, Zhu H, Qian X, et al. MRI Texture Analysis for Differentiating Nonfunctional Pancreatic Neuroendocrine Neoplasms From Solid Pseudopapillary Neoplasms of the Pancreas. Acad Radiol. 2020;27(6):815–823. doi: 10.1016/j.acra.2019.07.012
- He M, Liu Z, Lin Y, et al. Differentiation of atypical non functional pancreatic neuroendocrine tumor and pancreatic ductal adenocarcinoma using CT based radiomics. Eur J Radiol. 2019;117:102–111. doi: 10.1016/j.ejrad.2019.05.024
- An P, Zhang J, Li M, et al. Clinical Data CT Radiomics Based Model for Predicting Prognosis of Patients with Gastrointestinal Pancreatic Neuroendocrine Neoplasms (GP-NENs). Comput Math Methods Med. 2022;2022:4186305. doi: 10.1155/2022/4186305
- Song C, Wang M, Luo Y, et al. Predicting the recurrence risk of pancreatic neuroendocrine neoplasms after radical resection using deep learning radiomics with preoperative computed tomography images. Ann Transl Med. 2021;9(10):833. doi: 10.21037/atm-21-25
- Caruso D, Polici M, Rinzivillo M, et al. CT-based radiomics for prediction of therapeutic response to Everolimus in metastatic neuroendocrine tumors. Radiol Med. 2022;127(7):691–701. doi: 10.1007/s11547-022-01506-4
Arquivos suplementares