Методология тестирования и мониторинга программного обеспечения на основе технологий искусственного интеллекта для медицинской диагностики
- Авторы: Васильев Ю.А.1, Владзимирский А.В.1, Омелянская О.В.1, Арзамасов К.М.1, Четвериков С.Ф.1, Румянцев Д.А.1, Зеленова М.А.1
-
Учреждения:
- Научно-практический клинический центр диагностики и телемедицинских технологий
- Выпуск: Том 4, № 3 (2023)
- Страницы: 252-267
- Раздел: Оригинальные исследования
- URL: https://bakhtiniada.ru/DD/article/view/254067
- DOI: https://doi.org/10.17816/DD321971
- ID: 254067
Цитировать
Аннотация
Обоснование. Мировая сумма инвестиций в компании по разработке программного обеспечения на основе технологий искусственного интеллекта для медицинской диагностики составила 80 млн долларов в 2016 году, 152 млн долларов ― в 2017 и, ожидаемо, продолжает расти. Активная деятельность компаний-производителей программного обеспечения должна соответствовать существующим клиническим, биоэтическим, правовым и методологическим основам и стандартам. Как на национальном, так и на международном уровне не существует единых стандартов и протоколов проведения испытаний и мониторинга программного обеспечения на основе технологий искусственного интеллекта для медицинской диагностики.
Цель ― разработать универсальную методологию тестирования и мониторинга программного обеспечения на основе технологий искусственного интеллекта для медицинской диагностики, направленную на повышение его качества и внедрение в практическое здравоохранение.
Материалы и методы. В ходе аналитического этапа был проведён обзор литературы по базам данных PubMed и eLIBRARY. Практический этап включал апробацию разработанной методологии в рамках Эксперимента по использованию инновационных технологий в области компьютерного зрения для анализа медицинских изображений и дальнейшего применения в системе здравоохранения города Москвы.
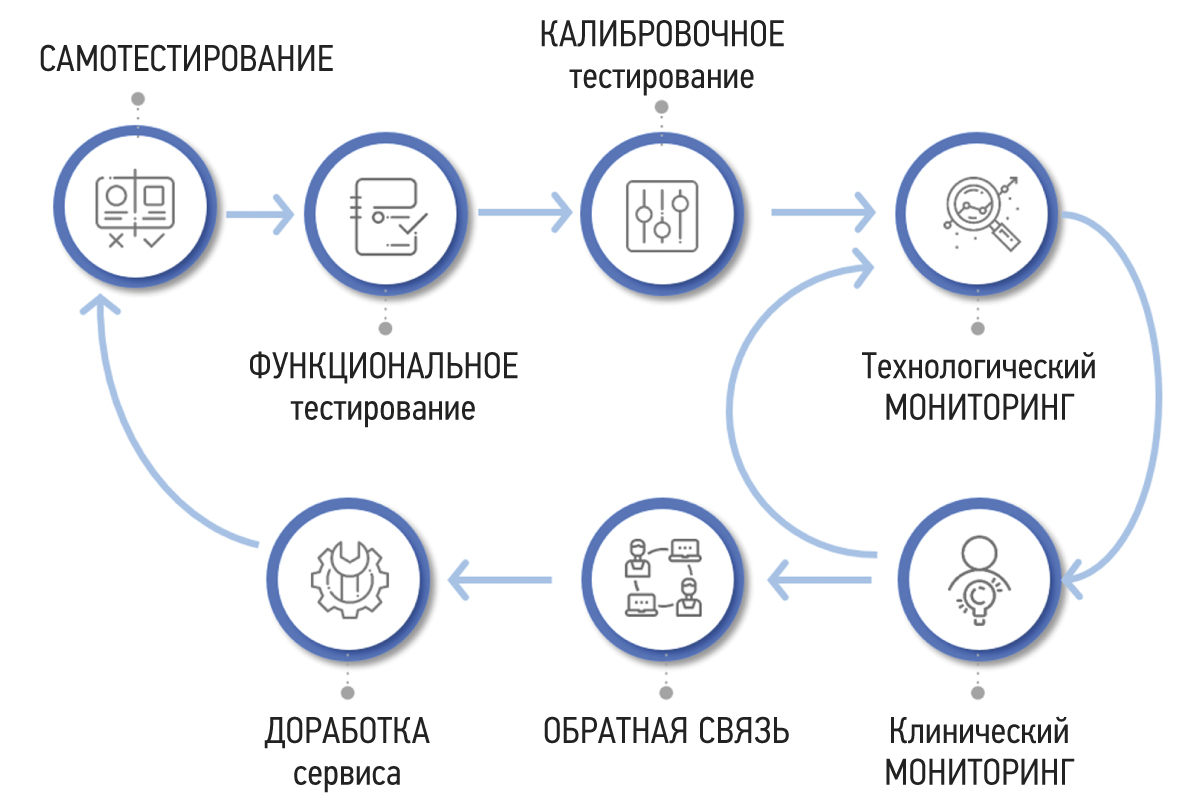
Результаты. Разработана методология тестирования и мониторинга программного обеспечения на основе технологий искусственного интеллекта для медицинской диагностики, направленная на повышение качества данного программного обеспечения и его внедрение в практическое здравоохранение. Методология состоит из 7 этапов: самотестирование, функциональное тестирование, калибровочное тестирование, технологический мониторинг, клинический мониторинг, обратная связь и доработка.
Заключение. Отличительными особенностями методологии являются цикличность этапов тестирования, мониторинга и доработки программного обеспечения, приводящие к постоянному повышению его качества, наличие подробных требований к результатам его работы, участие врачей в его оценке. Методология позволит разработчикам программного обеспечения достичь высоких результатов и продемонстрировать достижения в различных направлениях, а пользователям ― сделать осознанный и уверенный выбор среди программ, прошедших независимую и всестороннюю проверку качества.
Полный текст
Открыть статью на сайте журналаОб авторах
Юрий Александрович Васильев
Научно-практический клинический центр диагностики и телемедицинских технологий
Email: VasilevYA1@zdrav.mos.ru
ORCID iD: 0000-0002-0208-5218
SPIN-код: 4458-5608
канд. мед. наук
Россия, МоскваАнтон Вячеславович Владзимирский
Научно-практический клинический центр диагностики и телемедицинских технологий
Email: VladzimirskijAV@zdrav.mos.ru
ORCID iD: 0000-0002-2990-7736
SPIN-код: 3602-7120
д-р мед. наук
Россия, МоскваОльга Васильевна Омелянская
Научно-практический клинический центр диагностики и телемедицинских технологий
Email: OmelyanskayaOV@zdrav.mos.ru
ORCID iD: 0000-0002-0245-4431
SPIN-код: 8948-6152
Россия, Москва
Кирилл Михайлович Арзамасов
Научно-практический клинический центр диагностики и телемедицинских технологий
Email: ArzamasovKM@zdrav.mos.ru
ORCID iD: 0000-0001-7786-0349
SPIN-код: 3160-8062
канд. мед. наук
Россия, МоскваСергей Федорович Четвериков
Научно-практический клинический центр диагностики и телемедицинских технологий
Email: ChetverikovSF@zdrav.mos.ru
ORCID iD: 0000-0002-3097-8881
SPIN-код: 3815-8870
канд. тех. наук
Россия, МоскваДенис Андреевич Румянцев
Научно-практический клинический центр диагностики и телемедицинских технологий
Автор, ответственный за переписку.
Email: x.radiology@mail.ru
ORCID iD: 0000-0001-7670-7385
SPIN-код: 8734-2085
Россия, Москва
Мария Александровна Зеленова
Научно-практический клинический центр диагностики и телемедицинских технологий
Email: ZelenovaMA@zdrav.mos.ru
ORCID iD: 0000-0001-7458-5396
SPIN-код: 3823-6872
Россия, Москва
Список литературы
- Oakden-Rayner L., Palme L.J. Artificial intelligence in medicine: Validation and study design. In: Ranschart E., Morozov S., Algra P., eds. Artificial intelligence in medical imaging. Cham: Springer, 2019. Р. 83–104.
- Морозов С.П., Зинченко В.В., Хоружая А.Н., и др. Стандартизация искусственного интеллекта в здравоохранении: Россия выходит в лидеры // Врач и информационные технологии. 2021. № 2. С. 12–19. doi: 10.25881/18110193_2021_2_12
- Мелдо А.А., Уткин Л.В., Трофимова Т.Н. Искусственный интеллект в медицине: современное состояние и основные направления развития интеллектуальной диагностики // Лучевая диагностика и терапия. 2020. № 1. С. 9–17. doi: 10.22328/2079-5343-2020-11-1-9-17
- Зинченко В.В., Арзамасов К.М., Четвериков С.Ф., и др. Методология проведения пострегистрационного клинического мониторинга для программного обеспечения с применением технологий искусственного интеллекта // Современные технологии в медицине. 2022. Т. 14, № 5. С. 15–25. doi: 10.17691/stm2022.14.5.02
- Tanguay W., Acar P., Fine B., et al. Assessment of radiology artificial intelligence software: A validation and evaluation framework // Can Assoc Radiol J. 2023. Vol. 74, N 2. Р. 326–333. doi: 10.1177/08465371221135760
- Kohli A., Jha S. Why CAD failed in mammography // J Am Coll Radiol. 2018. Vol. 15, N 3, Pt. B. Р. 535–537. doi: 10.1016/j.jacr.2017.12.029
- Recht M.P., Dewey M., Dreyer K., et al. Integrating artificial intelligence into the clinical practice of radiology: Challenges and recommendations // Eur Radiol. 2020. Vol. 30, N 6. Р. 3576–3584. doi: 10.1007/s00330-020-06672-5
- Higgins D.C., Johner C. Validation of artificial intelligence containing products across the regulated healthcare industries // Ther Innov Regul Sci. 2023. Vol. 57, N 4. Р. 797–809. doi: 10.1007/s43441-023-00530-4
- Rudolph J., Schachtner B., Fink N., et al. Clinically focused multi-cohort benchmarking as a tool for external validation of artificial intelligence algorithm performance in basic chest radiography analysis // Sci Rep. 2022. Vol. 12, N 1. Р. 12764. doi: 10.1038/s41598-022-16514-7
- Allen B., Dreyer K., Stibolt R., et al. Evaluation and real-world performance monitoring of artificial intelligence models in clinical practice: Try it, buy it, check it // J Am Coll Radiol. 2021. Vol. 18, N 11. Р. 1489–1496. doi: 10.1016/j.jacr.2021.08.022
- Strohm L., Hehakaya C., Ranschaert E.R., et al. Implementation of artificial intelligence (AI) applications in radiology: Hindering and facilitating factors // Eur Radiol. 2020. Vol. 30, N 10. Р. 5525–5532. doi: 10.1007/s00330-020-06946-y
- Sohn J.H., Chillakuru Y.R., Lee S., et al. An open-source, vender agnostic hardware and software pipeline for integration of artificial intelligence in radiology workflow // J Digit Imaging. 2020. Vol. 33, N 4. Р. 1041–1046. doi: 10.1007/s10278-020-00348-8
- Wichmann J.L., Willemink M.J., De Cecco C.N. Artificial intelligence and machine learning in radiology: Current state and considerations for routine clinical implementation // Invest Radiol. 2020. Vol. 55, N 9. Р. 619–627. doi: 10.1097/RLI.0000000000000673
- Larson D.B., Harvey H., Rubin D.L., et al. Regulatory frameworks for development and evaluation of artificial intelligence-based diagnostic imaging algorithms: Summary and recommendations // J Am Coll Radiol. 2021. Vol. 18, N 3, Pt. A. Р. 413–424. doi: 10.1016/j.jacr.2020.09.060
- Milam M.E., Koo C.W. The current status and future of FDA-approved artificial intelligence tools in chest radiology in the United States // Clin Radiol. 2023. Vol. 78, N 2. Р. 115–122. doi: 10.1016/j.crad.2022.08.135
- De Silva D., Alahakoon D. An artificial intelligence life cycle: From conception to production // Patterns (NY). 2022. Vol. 3, N 6. Р. 100489. doi: 10.1016/j.patter.2022.100489
- Cerdá-Alberich L., Solana J., Mallol P., et al. MAIC-10 brief quality checklist for publications using artificial intelligence and medical images // Insights Imaging. 2023. Vol. 14, N 1. Р. 11. doi: 10.1186/s13244-022-01355-9
- Vasey B., Novak A., Ather S., et al. DECIDE-AI: A new reporting guideline and its relevance to artificial intelligence studies in radiology // Clin Radiol. 2023. Vol. 78, N 2. Р. 130–136. doi: 10.1016/j.crad.2022.09.131
- Регламент подготовки наборов данных с описанием подходов к формированию репрезентативной выборки данных. Москва: Научно-практический клинический центр диагностики и телемедицинских технологий Департамента здравоохранения города Москвы, 2022. 40 с. (Лучшие практики лучевой и инструментальной диагностики; Часть 1).
- Четвериков С.Ф., Арзамасов К.М., Андрейченко А.Е., и др. Подходы к формированию выборки для контроля качества работы систем искусственного интеллекта в медико-биологических исследованиях // Современные технологии в медицине. 2023. Т. 15, № 2. С. 19–27. doi: 10.17691/stm2023.15.2.02
- Морозов С.П., Владзимирский А.В., Кляшторный В.Г., и др. Клинические испытания программного обеспечения на основе интеллектуальных технологий (лучевая диагностика). Москва: Научно-практический клинический центр диагностики и телемедицинских технологий Департамента здравоохранения города Москвы, 2019. 33 с.
- Kim D.W., Jang H.Y., Kim K.W., et al. Design characteristics of studies reporting the performance of artificial intelligence algorithms for diagnostic analysis of medical images: Results from recently published papers // Korean J Radiol. 2019. Vol. 20, N 3. Р. 405–410. doi: 10.3348/kjr.2019.0025
Дополнительные файлы