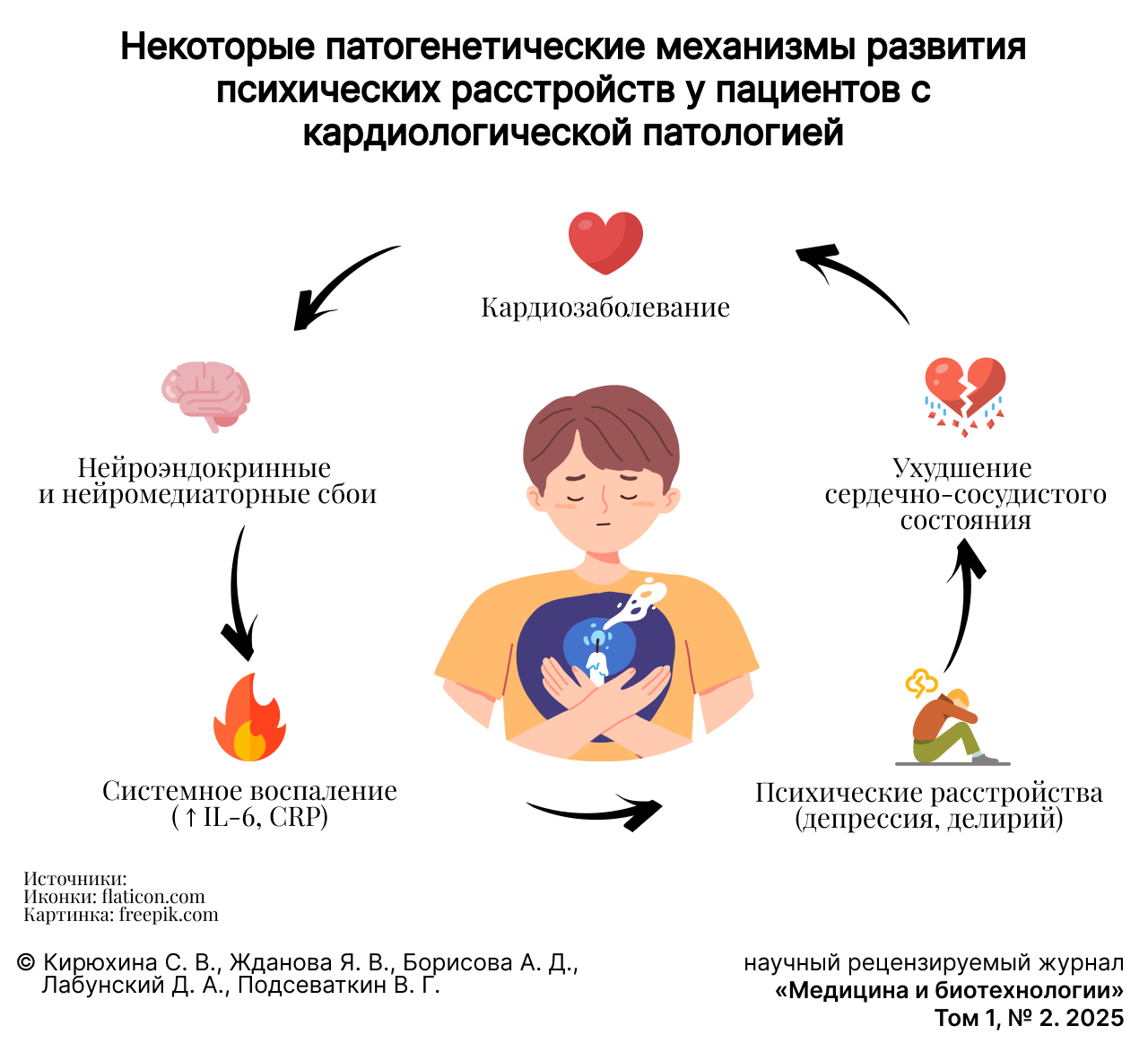
Некоторые патогенетические механизмы развития психических расстройств у пациентов с кардиологической патологией
- Авторы: Кирюхина С.В.1, Жданова Я.В.1, Борисова А.Д.1, Лабунский Д.А.1, Подсеваткин В.Г.1
-
Учреждения:
- Национальный исследовательский Мордовский государственный университет
- Выпуск: Том 1, № 2 (2025)
- Страницы: 140-153
- Раздел: Патологическая физиология
- Статья получена: 06.05.2025
- Статья одобрена: 14.05.2025
- Статья опубликована: 23.06.2025
- URL: https://bakhtiniada.ru/3034-6231/article/view/290578
- DOI: https://doi.org/10.15507/3034-6231.001.202502.140-153
- EDN: https://elibrary.ru/mjynni
- ID: 290578
Цитировать
Полный текст
Аннотация
Введение. Проблема психических расстройств у пациентов с кардиологическими заболеваниями в настоящий момент является крайне актуальной. Развивающиеся психические расстройства значительно утяжеляют течение и ухудшают прогноз кардиологического заболевания. Эти состояния существенно снижают качество жизни пациентов, замедляют реабилитацию и увеличивают риск повторных госпитализаций. Цель обзора – проанализировать современные данные о патогенетических механизмах психических расстройств у пациентов с кардиологической патологией и выявить их влияние на течение и исходы заболеваний.
Материалы и методы. Проанализированы российские и зарубежные публикации о коморбидной психической и кардиологической патологии за период 2003–2025 гг. Для поиска литературных источников использовались ресурсы: ScienceDirect, CyberLeninka, JournalDoctor.Ru, Springer.
Результаты исследования. Депрессия диагностируется у 15–20 % пациентов с сердечно-сосудистыми заболеваниями, а тревога перед кардиологической операцией – у 55 %. Женщины молодого возраста, а также лица с нестабильной стенокардией и инфарктом миокарда имеют более высокий риск развития депрессивных состояний. Наибольшую значимость в развитии тревожно-депрессивного синдрома имеет дисфункция лобных отделов головного мозга. Послеоперационный делирий встречается у 26–52 % пациентов в зависимости от вида операции и является результатом гипоксии, гиперкапнии и воспалительных процессов. Основными патогенетическими механизмами являются нейрогормональные изменения, дисфункция эндотелия, нарушения в нейротрансмиттерных системах и системные воспалительные реакции. Частота различных клинических типов послеоперационной мозговой дисфункции в кардиохирургии варьируется: периоперационный мозговой инсульт выявляется в 1–9 % случаев операций; симптоматический делирий в раннем послеоперационном периоде наблюдается у 7–52 % пациентов; отсроченные когнитивные нарушения фиксируются у 10–80 % пациентов.
Обсуждение и заключение. Особый интерес представляет взаимосвязь между психическими расстройствами и патофизиологическими процессами, сопровождающими кардиологическую патологию. Нейрогормональные изменения, воспалительные реакции, нарушение гематоэнцефалического барьера, а также дисфункция нейротрансмиттерных систем усугубляют течение как психических, так и кардиологических заболеваний. Данные механизмы создают замкнутый круг, где психические расстройства усиливают тяжесть сердечно-сосудистых заболеваний, а соматическая патология, в свою очередь, способствует усугублению психического состояния. Исследование патогенетических механизмов психических заболеваний у пациентов с кардиологической патологией имеет не только теоретическое, но и практическое значение для разработки новых персонализированных подходов лечения, ранней диагностики и коррекции выявленных расстройств.
Полный текст
Введение
Коморбидная патология представляет собой одновременное существование у пациента двух и более заболеваний, протекающих в одно время или являющихся осложнением течения основного заболевания или его лечения. Развитие коморбидной патологии обусловлено высокой распространенностью и общностью патогенетических механизмов многих патологических состояний. В условиях коморбидности заболевания приобретают атипичное и более тяжелое течение, повышается риск развития осложнений, снижается эффективность лечебных мероприятий.
Среди множества коморбидных патологий значительный интерес представляет изучение и сопоставление патогенетических механизмов психических и сердечно-сосудистых заболеваний. Высокая распространенность данных патологий, их экономическая и социальная значимость, гетерогенность клинической симптоматики, неблагоприятное прогрессирующее течение, а также частое сочетание кардиологических нарушений с различными формами психопатологических расстройств определяет актуальность изучения общих патогенетических механизмов развития, что необходимо для разработки эффективных и безопасных профилактических и лечебных мероприятий.
Одним из факторов риска развития комобридных психических и сердечно-сосудистых заболеваний является возраст, поскольку в детском и старческом возрасте число таких заболеваний наиболее высоко.
Цель исследования – проанализировать основные патогенетические механизмы, лежащие в основе развития психических расстройств у пациентов с сердечно-сосудистыми заболеваниями, выявить основные предикторы развития психических расстройств, изучить специфику послеоперационных психических нарушений.
Материалы и методы
На основе изучения электронных российских и зарубежных публикаций проведен теоретический анализ патогенетических механизмов развития психических расстройств у пациентов с кардиологической патологией. Для поиска литературных источников использовались ресурсы: https://www.sciencedirect.com/, https://cyberleninka.ru/, https://journaldoctor.ru/, https://link.springer.com/. Процитировано 27 отечественных и 23 зарубежных источника.
Результаты исследования
Патогенетические механизмы психоэмоциональных расстройств в пред- и послеоперационном периоде у пациентов кардиологического профиля
Депрессия все чаще определяется как расстройство эмоций. Основными симптомами депрессии являются потеря удовольствия или интереса от привычной жизни и деятельности, чрезмерно пониженное настроение, двигательная и идеаторная заторможенность, нарушения сна, вегетативные расстройства, благодаря чему можно полагать, что нарушенная регуляция эмоций может влиять на дальнейшее развитие расстройства [1; 2].
Многочисленные исследования выявили факторы риска развития депрессивных расстройств у пациентов с сердечно-сосудистыми заболеваниями. Депрессиям наиболее часто подвержены лица молодого возраста, особенно женщины, а также пациенты с ранее диагностированными случаями депрессии и острым коронарным синдромом [3; 4]. Чаще всего депрессия возникает у пациентов с нестабильной стенокардией и инфарктом миокарда [3; 5].
Близость кардиологической операции является фактором, провоцирующим определенные когнитивные и эмоциональные реакции пациента [6]. Согласно данным исследователей, среди пациентов с заболеваниями сердца депрессивные расстройства встречаются в 15–20 % случаев [7]. Доказано, что предоперационная тревожность является существенным фактором, предопределяющим исход операции, а именно, в случае повторной госпитализации после аортокоронарного шунтирования. Такая связь между депрессией и неблагоприятным прогнозом после операции на сердце указывает на то, что депрессия может проявляться до и продолжаться после операции, причем ее проявления у мужчин и у женщин различны [7; 8]. Следует отметить, что отягощающими факторами развития депрессивных расстройств у пациентов с кардиологической патологией являются сопутствующие инфекционные заболевания, а также острые сосудистые нарушения [9; 10]. У 34 % пациентов с заболеваниями сердца наблюдаются симптомы депрессии, а 55 % больных сообщают о тревоге перед операцией. Послеоперационная депрессия влияет на поведение пациентов. Рост числа визитов к врачам по поводу депрессивных расстройств приводит к существенному увеличению финансовых расходов на лечение [11; 12].
Для большинства пациентов операция на сердце является опасной для жизни, так как из-за возникающих послеоперационных расстройств у некоторых пациентов значительно тормозятся процессы реабилитации. Следует учитывать, что применяемые кардиологические препараты могут по-разному влиять на психические процессы, эмоциональную сферу и течение депрессии [13]. Результаты, полученные в ходе исследования, позволяют сделать следующие выводы: у 75 % пациентов, перенесших аортокоронарное шунтирование, проявлялись симптомы тревоги или депрессии, среди них у 28 % пациентов были выявлены значительные расстройства адаптации со снижением настроения, тревогой или со смешанным тревожно-депрессивным настроением, при этом симптомы депрессии и высокий уровень тревожности чаще встречались у лиц женского пола [13; 14].
Имеются дополнительные данные о распространенности депрессии у пациентов до и после проведенной операции на сердце. Депрессия выявлялась у 27–47 % пациентов, которым была запланирована операция на сердце, и у 19–61 % после операции. Доказано, что у пациентов с тревогой и депрессией сосудистое повреждение, связанное непосредственно с хирургическим вмешательством, определяется на фоне уже существующих физиологических патологий, включая нейрогормональные изменения, дисфункцию эндотелия сосудов и нестабильность возбудимости миокарда, тем самым определяя дополнительный риск для гомеостатического и циркуляторного баланса. Известно, что предоперационный стресс может быть вызван нарушением гемостаза и имеющейся дислипопротеинемией [15].
В развитии тревожно-депрессивного синдрома наибольшую значимость имеет дисфункция лобных отделов головного мозга. Известным фактом является взаимосвязь стриарного комплекса и дорсолатеральной лобной коры, которая способствует формированию положительных эмоций при достижении поставленной цели в ходе какой-либо деятельности [16; 17]. В случае нарушения данной связи в результате феномена разобщения происходит снижение положительного эмоционального фона, что и будет приводить к развитию депрессии [16; 18].
Возникновению депрессии после операции на сердце может способствовать дисбаланс вегетативной нервной системы, проявляющийся в преобладании симпатической активности, а также воспалительный процесс, связанный с повышенным уровнем провоспалительных цитокинов, индуцирующих нейровоспаление1; изменение пероксидазной функции комплекса цитохрома С с кардиолипином; нарушение функции гипоталамо-гипофизарно-надпочечниковой оси, что приводит к усилению стрессовых реакций и кортизолового ответа [19; 20].
С-реактивный белок (СРБ) – это острофазный белок, уровень которого повышается во время воспаления. Благодаря исследованиям Yang L. и соавт. доказано, что увеличение уровня СРБ является независимым предиктором депрессии у пациентов, перенесших операцию на сердце. Полученные клинические результаты могут помочь выявить потенциальные цели для улучшения исходов у больных с депрессией, перенесших данную операцию [21].
Lewis Ch. с соавт. утверждают, что у пациентов, имеющих в анамнезе депрессию, троекратно повышается риск возникновения делирия после проведенного кардиохирургического вмешательства [22].
Роль некоторых патогенетических факторов в развитии послеоперационного делирия в области кардиохирургии
При проведении кардиохирургических операций делирий, развивающийся в послеоперационном периоде, является довольно частым психическим расстройством.
В соответствии с Международной классификацией болезней 10-го пересмотра делирий определяется как неспецифический органический синдром, характеризующийся одновременным нарушением сознания и внимания, восприятия, мышления, памяти, психомоторного поведения, эмоций, цикличности сна и бодрствования2. У пациентов с сердечно-сосудистыми заболеваниями после кардиохирургических операций часто наблюдается развитие послеоперационного делирия [23].
Диагностическое и статистическое руководство Американской психиатрической ассоциации пятого издания (DSM-5) отмечает следующие основные диагностические критерии делирия: острое начало нарушения внимания и сознания, имеющее волнообразное течение, нарушение когнитивных процессов; предположительно, эти расстройства могут быть вызваны соматическим заболеванием, интоксикацией психоактивными веществами, а также побочным эффектом от приема лекарственных средств [24].
В метаанализе 2021 г. установлено, что ряд факторов, таких как стеноз сонной артерии, наличие сахарного диабета, гипертония, процент фракции выброса левого желудочка, предшествующие когнитивные расстройства и III или IV классы классификации по NYHA (New York Heart Association) являются значимыми рисками для развития послеоперационного делирия [25].
Пасюга В. В. и соавт. утверждают, что частота развития делирия в послеоперационном периоде в среднем составляет 26–52 %, и этот выявленный процент зависит от различных методов и критериев диагностики. Исследователи обнаружили, что частота возникновения делирия обусловлена видом оперативного вмешательства. Так, при выполнении операции аортокоронарного шунтирования без искусственного кровообращения определяется наименьшая частота развития делирия, которая составляет 4 %, а с использованием искусственного кровообращения она увеличивается до 13 %. Операции на клапанах сердца сопровождаются развитием делирия в 15 % случаев. Значительное возрастание риска развития данной патологии выявляется после комбинированных операций на сердце – 26 %, что связано с повышением сложности и длительности хирургического вмешательства. Достаточно высокий процент возникновения делирия отмечается после проведения транскатетерной имплантации аортального клапана – 18 %, а также после операции на корне аорты, восходящей аорте и дуге аорты – 21 %. Умеренный процент делирия наблюдается после операции при врожденных пороках сердца – 8 %, и после каротидной эндартерэктомии – 2 % [26].
Stessel B. с коллегами, проведя исследование, утверждают, что послеоперационный делирий в отделении интенсивной терапии был зафиксирован у 5 пациентов (8,6 %) после проведения эндоскопического аортокоронарного шунтирования [27].
Патогенетически значимыми факторами в развитии послеоперационного делирия являются гипоксия и гиперкапния, которые приводят к нарушениям в нейротрансмиттерных системах – чрезмерная активация домафинергической, глутаминергической и норадренергической систем, снижение холинергической активности, дисбаланс серотонинергической и ГАМК-ергической активности [28; 29].
На протяжении долгого времени ученые наблюдали, что стресс и повышенная концентрация циркулирующих глюкокортикоидов способны оказывать неблагоприятное влияние на функционирование головного мозга, провоцируя развитие психических расстройств, в частности делирия. Это явление обусловлено тем, что в гиппокампе и лобной доли находятся глюкокортикоидные рецепторы. Данные структуры мозга играют важнейшую роль в регуляции когнитивных процессов. Нарушение их работы под воздействием избытка глюкокортикоидов могут приводить к ухудшению когнитивных функций, эмоциональной нестабильности и другим расстройствам психики. Mu D. L. с соавт. предполагают, что повышенная концентрация кортизола в сыворотке крови ассоциируется с увеличенным риском развития послеоперационного делирия, однако для них неясно, является ли эта связь причинной или обусловлена другими факторами. Также следует проводить дифференциальную диагностику сердечно-сосудистых расстройств с невротическими симптомами. Особенно затруднительны диагностические аспекты болевого синдрома, в частности ангинозной боли. Гиподиагностика стенокардии может нести прямую угрозу для жизни пациента [30; 31].
В 2013 г. Kazmierski J. с соавт., проведя проспективное когортное исследование, выяснили, что у пациентов с повышенным уровнем кортизола до операции аортокоронарного шунтирования в разы повышается риск развития послеоперационного делирия. Также они установили, что пациенты, которым до операции был поставлен диагноз «Большое депрессивное расстройство», имеют значительно более высокий уровень кортизола в послеоперационный период по сравнению с пациентами, не страдающими этим расстройством. Следовательно, большое депрессивное расстройство может способствовать развитию делирия в послеоперационном периоде. Данное исследование позволяет предположить, что повышенный уровень кортизола может быть причиной, а не следствием послеоперационного делирия [32].
Немаловажная роль в развитии делирия отводится воспалению. Стресс, связанный с кардиохирургическим вмешательством, особенно при применении искусственного кровообращения во время операции, способствует формированию в организме человека системной воспалительной реакции, в результате чего повышенный уровень цитокинов может привести к дисфункции эндотелия сосудов и нарушению гематоэнцефалического барьера [33; 34].
Интерлейкин-6 (IL-6) является важным фактором воспаления. Благодаря исследованиям Liu X. с коллегами (2018 г.) установлено, что у пациентов с послеоперационным делирием существенно повышался показатель IL-6 [33].
В 2021 г. Lv X. Ch. и соавт. обнаружили, что у пациентов с острым расслоением аорты, перенесших хирургическое вмешательство, уровень IL-6 в плазме крови, измеренный в разные отрезки времени (до операции, через 24 и 48 ч после операции) коррелировал с развитием послеоперационного делирия. Также они установили, что повышенная концентрация IL-6 в плазме крови рассматривается как потенциальный биомаркер для прогнозирования вероятности развития послеоперационного делирия у пациентов, перенесших кардиохирургическое вмешательство. Следует особо учитывать риски фатальных исходов у пациентов кардиологического профиля с отягощающей сопутствующей патологией, особенно с метаболическими нарушениями при сахарном диабете [35; 36].
Современные исследования подтвердили тесную связь уровня сывороточной нейронспецифической енолазы (NSE) с развитием послеоперационного делирия и обнаружением фосфорилированной тяжелой субъединицы нейрофиламента (pNF-H), которая служит косвенным маркером аксонального повреждения центральной нервной системы. Это позволяет сделать вывод, что NSE может отражать как возникновение послеоперационного делирия, так и степень его тяжести [37].
Имеются данные, подтверждающие провоцирование послеоперационного делирия при кардиохирургических операциях с применением анестезии на основе кетамина и пропофола [38]. Также предиктором развития послеоперационного делирия может являться гемотрансфузия эритроцитарной массы и свежезамороженной плазмы [26].
В одном из исследований доказано, что снижение предоперационного мозгового кровотока в островковой доле, измеренное с помощью однофотонной эмиссионной компьютерной томографии, является значимым предиктором развития послеоперационного делирия у пациентов с тяжелым аортальным стенозом, которые перенесли транскатетерную аортальную имплантацию [39].
Mahanna-Gabrielli E. с коллегами выдвинули гипотезу о том, что генотип риска GG по SNP rs10830963, связанному с рецептором мелатонина 1B, может играть важную роль в возникновении послеоперационного делирия у пациентов, перенесших операцию на аортальном клапане [40].
В исследовании, проведенном Ogawa M. с соавт., послеоперационный делирий оказался независимым предиктором развития послеоперационной слабости у пациентов, перенесших кардиохирургическое вмешательство. Как послеоперационная слабость, так и послеоперационный делирий продемонстрировали тесную связь с развитием крупных неблагоприятных сердечно-сосудистых событий в течение года после операции. Однако послеоперационный делирий оказался более значимым прогностическим фактором таких событий, по сравнению с послеоперационной слабостью [41].
Послеоперационный делирий оказывает негативное влияние на метаболизм нейронов, нарушая их активность, что со временем приводит к прогрессирующему снижению когнитивных функций, функциональной дегенерации и ухудшению общего прогноза. Этот факт подчеркивает важность ранней диагностики, профилактики и своевременного лечения послеоперационного делирия для минимизации последствий и улучшения качества жизни пациентов.
Патофизиологические механизмы когнитивных нарушений после кардиохирургических операций
Постнов В. Г. с соавт. предложили классификацию церебральных осложнений, возникающих после кардиохирургических операций, которая основывается на временных рамках появления неврологических нарушений. К ранним послеоперационным осложнениям относятся нервно-психические расстройства, такие как острые фокальные нарушения мозгового кровообращения ишемического и геморрагического типов, а также острые психопродуктивные расстройства. В госпитальном послеоперационном периоде наблюдаются отсроченные постгипоксические и метаболические энцефалопатии [42; 43].
Послеоперационная мозговая дисфункция представляет собой изменение структурного и функционального состояния головного мозга в основном сосудистого происхождения, которое может возникать в ходе хирургического вмешательства или в ранний послеоперационный период. Это состояние проявляется в виде временных или постоянных нарушений функций нервной системы [42; 44].
В период с 2010 по 2013 гг. на базе Военно-медицинской академии им. С. М. Кирова и Санкт-Петербургского государственного педиатрического медицинского университета были проведены взаимодополняющие исследования – экспериментальные и клинические. Они позволили выделить патогенетические механизмы послеоперационной мозговой дисфункции и классифицировать ее клинические формы: периоперационный мозговой инсульт; симптоматический делирий в раннем послеоперационном периоде; отсроченные когнитивные нарушения [42; 45].
Первые две формы развиваются вследствие острого повреждения нейронов и нейроглии, тогда как отсроченные когнитивные нарушения связаны с постепенным поражением нервных клеток [42; 46].
Учитывая сходство в патогенезе и значительное влияние на результаты лечения, периоперационный мозговой инсульт и симптоматический делирий в раннем послеоперационном периоде могут быть объединены под термином «острые клинические формы послеоперационной мозговой дисфункции».
Изменения гемодинамики при кардиохирургических операциях в условиях искусственного кровообращения приводят к повреждениям сосудов как микроцикуляторного, так и макроциркуляторного русла, вследствие чего повышается риск образования крупноочагового некроза нервной ткани, которое проявляется периоперационным мозговым инсультом [47].
Важно отметить, что повреждение сосудов микроциркуляторного русла в сочетании с отсроченным повреждением нервной ткани постепенно приводит к развитию стойких когнитивных нарушений. Эти изменения могут проявиться спустя несколько дней или даже недель после проведенной операции и сохраняются в течение длительного времени, значительно влияя на общее состояние пациента.
Частота различных клинических типов послеоперационной мозговой дисфункции в кардиохирургии варьируется: периоперационный мозговой инсульт выявляется в 1–9 % случаев операций; симптоматический делирий в раннем послеоперационном периоде наблюдается у 7–52 % пациентов; отсроченные когнитивные нарушения фиксируются у 10–80 % пациентов [42].
В 2022 г. Цыган Н. В. с соавт. провели исследование частоты и структуры послеоперационной мозговой дисфункции при протезировании аортального клапана. В ходе комплексного периоперационного обследования пациентов, перенесших данную операцию, была проанализирована частота возникновения послеоперационной мозговой дисфункции и ее различных клинических форм. Общая частота появления послеоперационной мозговой дисфункции составила 41,2 % (47 пациентов) [48]. Среди ее клинических форм: острые клинические типы послеоперационной мозговой дисфункции наблюдались в 18,4 % случаев (21 пациент), периоперационный инсульт был зафиксирован в 1,7 % случаев (2 пациента), симптоматический делирий раннего послеоперационного периода диагностирован в 16,7 % случаев (19 пациентов), отсроченные когнитивные нарушения, выявленные на более поздних этапах послеоперационного наблюдения, отмечены в 28,6 % случаев (32 пациента из 112 обследованных, при этом из анализа были исключены 2 пациента с инсультом). Полученные результаты продемонстрировали, что когнитивные и неврологические нарушения после операции являются достаточно распространенными. При терапии пациентов с кардиологической патологией необходимо учитывать безопасность, нежелательные явления, противопоказания к применению, в том числе особенности влияния на психические и неврологические функции у антиаритмических препаратов Ic класса [48; 49].
Следует упомянуть факт, установленный Maekawa K., что у пожилых людей, которые перенесли операцию на сердце и столкнулись с постоперационным когнитивным расстройством, фиксируется снижение объема серого вещества в обеих структурах медиальной височной доли, а также обнаруживаются повреждения белого вещества мозга [50].
Обсуждение и заключение
Практическая значимость исследования заключается в возможности применения полученных данных для разработки персонализированных стратегий диагностики, профилактики и лечения психических расстройств у пациентов с кардиологической патологией.
Выявление ключевых патогенетических механизмов (нейрогормональный дисбаланс, воспаление, дисфункция нейротрансмиттерных систем) позволяет внедрять раннюю биохимическую и инструментальную диагностику (например, мониторинг уровня СРБ, IL-6, кортизола), что способствует своевременной коррекции нарушений.
Результаты исследования обосновывают необходимость мультидисциплинарного подхода, включающего консультации психиатров и неврологов на этапах предоперационной подготовки и реабилитации. Это поможет снизить частоту послеоперационных осложнений, сократить сроки госпитализации, улучшить качество жизни пациентов и уменьшить экономическую нагрузку на систему здравоохранения за счет снижения числа повторных госпитализаций.
1 Жомарт А. Алгоритмы, которые спасают сердца: ИИ в кардиологии // Научное сообщество студентов. Междисциплинарные исследования : сборник статей по материалам CCIV студенческой международной научно-практической конференции. Новосибирск, 09 января 2025 г. Новосибирск : ООО «Сибирская академическая книга», 2025. С. 62–66. https://elibrary.ru/jfeisb
2 МКБ 10 – Международная классификация болезней 10-го пересмотра. Классы M№-10/F00-F99/F00-F09/F05 [Электронный ресурс]. URL: https://mkb-10.com/index.php?pid=4024 (дата обращения: 15.04.2025).
Об авторах
Светлана Владимировна Кирюхина
Национальный исследовательский Мордовский государственный университет
Автор, ответственный за переписку.
Email: krsv55@mail.ru
ORCID iD: 0000-0002-9457-8756
SPIN-код: 1706-7617
Scopus Author ID: 26650047400
ResearcherId: AAB-2603-2022
https://orcid.org/0000-0002-9457-8756
доктор медицинских наук, профессор кафедры психиатрии, наркологии и неврологии
Россия, 430005, г. Саранск, ул. Большевистская, 68Яна Владимировна Жданова
Национальный исследовательский Мордовский государственный университет
Email: yantarchiik@yandex.ru
ORCID iD: 0009-0000-9138-9258
студент Медицинского института
Россия, 430005, г. Саранск, ул. Большевистская, 68Алина Дмитриевна Борисова
Национальный исследовательский Мордовский государственный университет
Email: alinazevajkina@gmail.com
ORCID iD: 0009-0005-9288-4732
студент Медицинского института
Россия, 430005, г. Саранск, ул. Большевистская, 68Дмитрий Александрович Лабунский
Национальный исследовательский Мордовский государственный университет
Email: dmitriylabunskiy@gmail.com
ORCID iD: 0000-0001-6629-6682
SPIN-код: 8136-5353
Scopus Author ID: 6504155528
кандидат медицинских наук, доцент, доцент кафедры психиатрии, наркологии и неврологии
Россия, 430005, г. Саранск, ул. Большевистская, 68Вячеслав Григорьевич Подсеваткин
Национальный исследовательский Мордовский государственный университет
Email: kafedrapsi1@yandex.ru
ORCID iD: 0000-0001-9416-5727
SPIN-код: 4518-6140
Scopus Author ID: 35084166500
https://orcid.org/0000-0001-9416-5727
доктор медицинских наук, профессор, профессор кафедры психиатрии, наркологии и неврологии
Россия, 430005, г. Саранск, ул. Большевистская, 68Список литературы
- Patron E., Messerotti Benvenuti S., Favretto G., Gasparotto R., Palomba D. Depression and Reduced Heart Rate Variability after Cardiac Surgery: the Mediating Role of Emotion Regulation. Autonomic Neuroscience: Basic and Clinical. 2014;180:53–58. https://doi.org/10.1016/j.autneu.2013.11.004
- Стяжкина Ю.А., Гришина И.Ф., Полетаева Н.Б., Перетолчина Т.Ф. Особенности психологического статуса у пациентов после коронарного шунтирования при разной продолжительности амбулаторного этапа реабилитации. Врач. 2025;36(4):54–59. https://doi.org/10.29296/25877305-2025-04-11
- Винокуров Е.В., Собенников В.С. Депрессия и кардиологические заболевания (обзор литературы). Acta Biomedica Scientifica. 2017;2(4):63–67. https://doi.org/10.12737/article_59fad516bdb3e0.52521063
- Кочеткова И.В., Трофимова Т.Г., Лыков Ю.А., Кухарчук А.Е. Клинико-прогностическое значение биомаркеров NT-proBNP и sST2 у пожилых пациентов с сердечной недостаточностью и сопутствующей патологией. Врач. 2025;(4):62–67. https://doi.org/10.29296/25877305-2025-04-13
- Бирюкова Д.А., Пронищева Е.А. Исследование междисциплинарного подхода к лечению пациентов с хронической сердечной недостаточностью: клинический аспект. Medicus. 2025;3(69):13–17. https://www.elibrary.ru/opzgpo
- Rymaszewska J., Kiejna A., Hadryś T. Depression and Anxiety in Coronary Artery Bypass Grafting Patients. European Psychiatry. 2003;18(4):155–160. https://doi.org/10.1016/s0924-9338(03)00052-x
- Stenman M., Sartipy U. Depression Screening in Cardiac Surgery Patients. Heart, Lung and Circulation. 2019;28(6):953–958. https://doi.org/10.1016/j.hlc.2018.04.298
- Кузьмина В.А., Кирюхина С.В. Особенности влияния комплексной терапии на динамику показателей гомеостаза у лиц, перенесших инсульт. Вестник психофизиологии. 2024;1:105–108. https://doi.org/10.34985/y8278-6658-6491-r
- Кирюхина С.В., Подсеваткин В.Г., Подъячева Е.Н., Корнев Н.С. Депрессивные состояния после перенесенной коронавирусной инфекции. Вестник психофизиологии. 2024;1:57–64. https://doi.org/10.34985/z2077-6023-0275-b
- Грецева Т.А., Еникеев Д.А., Шайдуллина Э.А., Джанбекова Л.М., Карпелевич В.С., Кужина А.Р. и др. Генетические модификации в кардиологии: роль CRISPR-Cas9 в терапии сердечно-сосудистых заболеваний. Клинический разбор в общей медицине. 2025;6(1):29–40. https://doi.org/10.47407/kr2024.6.1.00547
- Curcio N., Philpot L., Bennett M., Felius J., Powers M.B., Edgerton J. et al. Anxiety, Depression, and Healthcare Utilization 1 Year after Cardiac Surgery. The American Journal of Surgery. 2019;218(2):335–341. https://doi.org/10.1016/j.amjsurg.2018.12.009
- Кукина Г.Н., Кирюхина С.В., Лабунский Д.А. Подсеваткин В.Г., Рузавина Е.Ф. Изучение комплекса QRS у лиц с депрессивными расстройствами, страдающими ожирением и апноэ сна. Российский кардиологический журнал. 2023;28(S6):27. https://elibrary.ru/dxqwss
- Подсеваткин В.Г., Кирюхина С.В., Лабунский Д.А., Макарова К.О. Особенности влияния антигипертензивных препаратов на некоторые показатели психических функций у лиц в возрасте от 18 до 35 лет. Кардиоваскулярная терапия и профилактика. 2025;24(S6):22. https://doi.org/10.15829/1728-8800-2025-6S
- Labunskiy D., Kuzmin D., Baranov D., Kiryukhina S., Pavelkina V. Efficiacy of Pharmacotherapy in Patients with Hypothimic Mental Disorders Suffered from Covid-19 Infection. European Psychiatry. 2023;66(S1):S181. https://doi.org/10.1192/j.eurpsy.2023.435
- Pignay-Demaria V., Lespérance F., Demaria R.G., Frasure-Smith N., Perrault L.P. Depression and Anxiety and Outcomes of Coronary Artery Bypass Surgery. The Annals of Thoracic Surgery. 2003;75(1):314–321. https://doi.org/10.1016/S0003-4975(02)04391-6
- Медведева Л.А., Загорулько О.И., Белов Ю.В., Пешкова О.П., Богопольская О.М. Когнитивная послеоперационная дисфункция в кардиохирургии. Кардиология и сердечно-сосудистая хирургия. 2012;5(4):46–54. URL: https://clck.ru/3M3XtC
- Мазуров В.И., Тыренко В.В., Вахлевский В.В. Проблемы кардиоиммунологии в клинике внутренних болезней. Терапия. 2025;11(1):116–124. https://doi.org/10.18565/therapy.2025.1.116-124
- Сергачев А.В., Кирюхина С.В., Кукина Г.Н., Лабунский Д.А., Подсеваткин В.Г. Психическая и сердечно-сосудистая патология при COVID-19: особенности межлекарственных взаимодействий. Вестник психофизиологии. 2023;2:51–59. https://doi.org/10.34985/f7293-0255-4517-i
- Vu T., Smith J.A. The Pathophysiology and Management of Depression in Cardiac Surgery Patients. Frontiers in Psychiatry. 2023;14:1195028. https://doi.org/10.3389/fpsyt.2023.1195028
- Ромодин Л.А. Комплекс цитохрома c с кардиолипином. Часть 2. Структура и пероксидазная активность (обзор литературы). Вестник новых медицинских технологий. 2021;28(3):68–72. https://doi.org/10.24412/1609-2163-2021-3-68-72
- Yang L., Wang J., Zhang L., Hou J., Yuan X., Hu S. et al. Preoperative High-Sensitivity C-reactive Protein Predicts Depression in Patients Undergoing Coronary Artery Bypass Surgery: a Single-Center Prospective Observational Study. The Journal of Thoracic and Cardiovascular Surgery. 2012;144(2):500–505. https://doi.org/10.1016/j.jtcvs.2012.01.034
- Lewis C., Dokucu M.E., Brown C.H., Balmert L., Srdanovic N., Shaan Madhan A. et al. Postoperative but not Preoperative Depression is Associated with Cognitive Impairment after Cardiac Surgery: Exploratory Analysis of Data from a Randomized Trial. BMC Anesthesiology. 2022;22(1):157. https://doi.org/10.1186/s12871-022-01672-y
- Дик К.П., Мельник А.А., Пономарев И.А., Довлатова А.Т., Бусыгин И.Д., Мамонова А.Д и др. Клинические типы послеоперационного делирия у лиц, перенесших кардиохирургическую операцию. Психиатрия. 2025;23(1):28–38. https://doi.org/10.30629/2618-6667-2025-23-1-28-38
- O’Neal J.B., Shaw A.D. Predicting, Preventing, and Identifying Delirium after Cardiac Surgery. Perioperative Medicine (London, England). 2016;5:7. https://doi.org/10.1186/s13741-016-0032-5
- Chen H., Mo L., Hu H., Ou Y., Luo J. Risk Factors of Postoperative Delirium after Cardiac Surgery: a Meta-Analysis. Journal of Cardiothoracic Surgery. 2021;16(1):113. https://doi.org/10.1186/s13019-021-01496-w
- Пасюга В.В., Демин Д.А., Нудель И.Л., Демина Е.В., Кадыкова А.В., Тарасов Д.Г. и др. Периоперационные факторы риска развития делирия после плановых кардиоваскулярных вмешательств. Патология кровообращения и кардиохирургия. 2020;24(2):83–94. http://dx.doi.org/10.21688/1681-3472-2020-2-83-94
- Stessel B., Nijs K., Pelckmans C., Vandenbrande J., Ory J.-P., Yilmaz A. et al. Neurological Outcome after Minimally Invasive Coronary Artery Bypass Surgery (NOMICS): An Observational Prospective Cohort Study. Public Library of Science ONE. 2020;15(12):e0242519. https://doi.org/10.1371/journal.pone.0242519
- Алексеева А.В., Орлов Ф.В., Веденеева И.А., Голенков А.В. Послеоперационный делирий в кардиохирургии. Acta Medica Eurasica. 2023;2:85–100. https://doi.org/10.47026/2413-4864-2023-2-85-100
- Кирюхина С.В., Баранов Д.В., Лабунский Д.А., Юрасова Е.Ю., Колмыков В.А., Разгадова Е.А. Исследование эффективности лечения депрессивных расстройств с использованием комплекса – антидепрессант, иммунокорректор, антиоксидант и гипербарическая оксигенация. Современные проблемы науки и образования. 2022;3:120. https://doi.org/10.17513/spno.31779
- Mu D.L., Wang D.X., Li L.H., Shan G.-J., Li J., Yu Q.-J. et al. High Serum Cortisol Level is Associated with Increased Risk of Delirium after Coronary Artery Bypass Graft Surgery: a Prospective Cohort Study. Critical Care: the Official Journal of the Critical Care Forum. 2010;14(6):R238. https://doi.org/10.1186/cc9393
- Еремеев А.Г. Дифференциально-диагностические аспекты ангинозной боли (стенокардии) и распространенных фенотипов ангинозоподобной боли. Врач. 2025;36(4):34–41. https://doi.org/10.29296/25877305-2025-04-07
- Kazmierski J., Banys A., Latek J., Bourke J., Jaszewski R. Cortisol Levels and Neuropsychiatric Diagnosis as Markers of Postoperative Delirium: a Prospective Cohort Study. Critical Care: the Official Journal of the Critical Care Forum. 2013;17(2):R38. https://doi.org/10.1186/cc12548
- Liu X., Yu Y., Zhu S. Inflammatory Markers in Postoperative Delirium (POD) and Cognitive Dysfunction (POCD): A Meta-Analysis of Observational Studies. Public Library of Science ONE. 2018;13(4):e0195659. https://doi.org/10.1371/journal.pone.0195659
- Артемьев А.Д., Баранов Д.В., Кирюхина С.В., Подсеваткин В.Г., Лабунский Д.А., Колмыкова Н.А. Роль антидепрессантов в коррекции клинических эндокринных и нейротрансмиттерных нарушений при суицидальном поведении: поиск новых терапевтических траекторий. Вестник Биомедицина и социология. 2022;7(2):23–29. https://doi.org/10.26787/nydha-2618-8783-2022-7-2-23-29
- Lv X.C., Lin Y., Wu Q.S., Wang L., Hou Y.-T., Dong Y. et al. Plasma Interleukin-6 is a Potential Predictive Biomarker for Postoperative Delirium among Acute Type A Aortic Dissection Patients Treated with Open Surgical Repair. Journal of Cardiothoracic Surgery. 2021;16(1):146. https://doi.org/10.1186/s13019-021-01529-4
- Бондарь И.А., Шабельникова О.Ю. Риски сердечно-сосудистых фатальных исходов при различных клинических фенотипах у больных сахарным диабетом типа 2 в Новосибирской области. Врач. 2025;36(3):66–72. https://doi.org/10.29296/25877305-2025-03-12
- Mietani K., Hasegawa-Moriyama M., Inoue R., Ogata T., Shimojo N., Kurano M. et al. Elevated Neuron-Specific Enolase Level is Associated with Postoperative Delirium and Detection of Phosphorylated Neurofilament Heavy Subunit: A Prospective Observational Study. Public Library of Science ONE. 2021;16(11):e0259217. https://doi.org/10.1371/journal.pone.0259217
- Киреев С.С., Бадаква Т.Л., Чуканова О.А. Делирий в послеоперационном периоде (обзор литературы). Вестник новых медицинских технологий. Электронное издание. 2019;2:44–46. URL: https://clck.ru/3M4iPK
- Takeuchi M., Suzuki H., Matsumoto Y., Kikuchi Y., Takanami K., Wagatsuma T. et al. Prediction of the Development of Delirium after Transcatheter Aortic Valve Implantation using Preoperative Brain Perfusion SPECT. Public Library of Science ONE. 2022;17(11):e0276447. https://doi.org/10.1371/journal.pone.0276447
- Mahanna-Gabrielli E., Miano T.A., Augoustides J.G., Kim C., Bavaria J.E., Kofke W.A. Does the Melatonin Receptor 1B Gene Polymorphism Have a Role in Postoperative Delirium? Public Library of Science ONE. 2018;13(11):e0207941. https://doi.org/10.1371/journal.pone.0207941
- Ogawa M., Izawa K.P., Satomi-Kobayashi S., Tsuboi Y., Komaki K., Gotake Y. et al. Impact of Delirium on Postoperative Frailty and Long Term Cardiovascular Events after Cardiac Surgery. Public Library of Science ONE. 2017;12(12):e0190359. https://doi.org/10.1371/journal.pone.0190359
- Одинак М.М., Литвиненко И.В., Хубулава Г.Г., Цыган Н.В., Андреев Р.В., Пелешок А.С. и др. Послеоперационная мозговая дисфункция при хирургической коррекции приобретенных пороков клапанов сердца. Доктор.Ру. 2018;153(9):6–12. https://doi.org/10.31550/1727-2378-2018-153-9-6-12
- Labunskiy D., Kiryukhina S., Podsevatkin V. Autoimmune Encephalitis: Antibodies to Neurotransmitters, Ion Channels, Tumor Antigens. What Next? Journal of the Neurological Sciences. 2021;429:118799. https://doi.org/10.1016/j.jns.2021.118799
- Кирюхина С.В., Гулина О.В., Подсеваткин В.Г., Кукина Г.Н., Юрасова Е.Ю., Лабунский Д.А. и др. Анализ инвалидности вследствие органических психических расстройств за 2019 год по Республике Мордовия. Медико-социальная экспертиза и реабилитация. 2021;24(1):23–29. https://doi.org/10.17816/MSER56386
- Кирюхина С.В., Кукина Г.Н., Колмыков В.А., Подсеваткин В.Г., Лабунский Д.А., Баранов Д.В. и др. Совершенствование стационарного этапа медицинской и социальной реабилитации инвалидов вследствие органического поражения головного мозга с помощью комплексной терапии с использованием антиоксиданта и гипербарической оксигенации. Вестник Всероссийского общества специалистов по медико-социальной экспертизе, реабилитации и реабилитационной индустрии. 2021;2:14–23. https://doi.org/10.17238/issn1999-2351.2021.2.14-23
- Labunskiy D., Kiryukhina S., Podsevatkin V., Govsh E., Kolmyykov V. Hyperbaric Oxygenation of Autoimmune Manifestation in Coversational Disorders. European Psychiatry. 2021;64(S1):S147–S148. https://doi.org/10.1192/j.eurpsy.2021.404
- Цыган Н.В., Одинак М.М., Хубулава Г.Г., Цыган В.Н., Пелешок А.С., Андреев Р.В. и др. Послеоперационная мозговая дисфункция. Журнал неврологии и психиатрии им. С.С. Корсакова. 2017;117(4):34–39. https://doi.org/10.17116/jnevro20171174134-39
- Цыган Н.В., Рябцев А.В., Андреев Р.В., Сапожников К.В., Пелешок А.С., Одинак М.М. и др. Послеоперационная мозговая дисфункция при протезировании аортального клапана сердца. Доктор.Ру. 2022;21(4):53–59. https://doi.org/10.31550/1727-2378-2022-21-4-53-59
- Канорский С.Г., Шубик Ю.В. Антиаритмические препараты Ic класса в кардиологической практике. Врач. 2025;36(3):32–39. https://doi.org/10.29296/25877305-2025-03-06
- Maekawa K., Baba T., Otomo S., Morishita S., Tamura N. Low Pre-Existing Gray Matter Volume in the Medial Temporal Lobe and White Matter Lesions Are Associated with Postoperative Cognitive Dysfunction after Cardiac Surgery. Public Library of Science ONE. 2014;9(1):e87375. https://doi.org/10.1371/journal.pone.0087375
Дополнительные файлы